腾盛博药登陆港交所,市值150亿港元:在公共卫生、CNS等领域寻求全球首创、最佳疗法
摘要: 抗病毒等重大治疗市场持续诞生十亿美元级全球畅销产品。本文为IPO早知道原创作者|罗宾微信公众号|ipozaozhidao据IPO早知道消息,腾盛博药生物科技有限公司(下称“腾盛博药”)于7月13日正式

抗病毒等重大治疗市场持续诞生十亿美元级全球畅销产品。
本文为IPO早知道原创
作者|罗宾
微信公众号|ipozaozhidao
据IPO早知道消息,腾盛博药生物科技有限公司(下称“腾盛博药”)于7月13日正式以“2137”为证券代码在港交所主板挂牌上市。
腾盛博药在本次IPO中总计发行1.12亿股股份。其中,香港公开发售部分获约292倍超额认购,国际发售部分获约12倍超额认购。发行价为招股区间顶部的每股22.25港元。
截至9:40,腾盛博药市值约150亿港元。
成立于2017年的腾盛博药是一家中美两地的跨国生物医药公司,主要针对具有重大公共负担的疾病领域如乙肝病毒(HBV)、HIV、多重耐药(MDR)或广泛耐药性(XDR)革兰氏阴性菌感染等重大传染病,以及中枢神经系统(CNS)疾病的创新疗法。
自成立以来,腾盛博药总计完成3轮融资,坐拥博裕资本、通和毓承、ARCH Venture Partners、红杉中国、云锋基金、景顺投资、蓝池资本、GIC、高瓴、Capital Research and Management Company等一众知名投资方。
值得注意的是,在本次IPO发行中,博裕、红杉、云锋三家早期投资人,以及Invesco、UBS、RBC加拿大皇家、AIHC瓴健、Springhill 启峰、Athos、Sage、Valliance共计11家股东作为基石投资者再次给予腾盛博药支持。
红杉资本全球执行合伙人沈南鹏表示:“腾盛博药作为一家致力于提升公共卫生水平的生物科技创新企业,凭借一流的技术实力,长期以来专注于突破性药物的开发和上市,尤其重点针对容易引发重大公共卫生影响的疾病药物研发,体现了团队的使命感与担当。我们期待与腾盛博药共同为改善全球患者的健康状况而努力。”
云锋基金执行董事黄潇表示:“腾盛博药是中国乃至国际领先的专注治疗慢性疾病和感染性疾病的制药企业,其联合小核酸药物及疫苗共同治愈乙肝的治疗路径,已经初步显现功能性治愈的曙光,给中国的亿万乙肝病人带来了治愈的希望。同时,腾盛博药在新冠抗体、神经等药物方面也颇有建树。希望在腾盛博药的帮助下,惠及更多中国乙肝患者,为健康中国添砖加瓦。”
管理层对全球创新药品开发及商业化有深厚经验
腾盛博药创始人Hong博士在生物医药行业有超25年的经验。创业前,他曾任葛兰素史克(GSK.US)高级副总裁及传染病治疗部主管(2007至2018年),2009至2018年,Hong博士曾在葛兰素史克子公司ViiV Healthcare负责监督HIV治疗和预防疗法的研发工作并担任董事。
腾盛博药另一位执行董事兼总裁、大中华区总经理罗永庆同样有至少25年的医疗保健行业经验。2016至2020年,罗永庆曾在上海吉利德任全球副总裁及中国总经理,他作为吉利德科学(GILD.US)在中国的早期员工,主导了8个创新产品的开发、监管审查和上市,使产品在中国获得快速准入。罗永庆还曾任诺华(NVS.US)在大中华区制药组总经理及诺华在瑞士的全球总部资深品牌董事长。
腾盛博药首席医学官严立博士曾在葛兰素史克担任副总裁兼制药研发部首席医师,负责全球肿瘤学开发活动。此外,严博士在延世大学担任兼职教授,负责教学和研究工作。
首席财务官李安康博士曾任拓臻生物的首席财务官、高盛高华证券财务部执行总监及默沙东研发(中国)有限公司业务开发部主管。
高级副总裁徐连红博士为药物化学研发部负责人。徐博士曾是吉利德的药物化学部药物化学高级主管,于1998年5月至2018年4月负责领导抗病毒项目并开展药物化学研究及小分子药物发现,并从中研制出多款商业化药物。
Jean-Luc Samuel Francois GIRARDET博士同为腾盛博药高级副总裁,主管制药科学部。Girardet博士曾在Ardea Biosciences工作十余年,他于2007年获委任为该公司的研究运营副总裁,负责化学及制造控制部及转化科学。他还曾就任于Valeant Pharmaceuticals International,负责领导丙肝病毒和人体免疫缺陷病毒化学项目组,并管理过程化学部。
第三位高级副总裁兼生物制药部负责人为朱青博士,他曾在阿斯利康(AZN.US)附属公司MedImmnue担任多个职位,其中最后一个职位是主管兼病毒学组组长,负责抗病毒项目的研究和开发。在此之前,她曾是诺华的一名科学家,自2006年起负责转化研究。她还曾是美国研究机构Fox Chase Cancer Center的博士后研究员。
Lisa Trivison BECK为博盛腾药另一位主管商务拓展和投资组合策略的高级副总裁。Beck曾为Alexion Pharmaceuticals(ALXN.US)的交易及联盟管理负责人。她还曾在1991年至2015年担任葛兰素史克的投资组合管理总监,负责多项疗法的业务开发、Stiefel皮肤科项目的投资组合管理以及皮肤科产品的临床研究和项目管理。
创新疗法将大力解决抗病毒、CNS领域未满足需求
传染病是全球医药市场第三大治疗领域,而创新疗法正在主导传染病治疗市场的增长,并将作出很大贡献。传染病创新疗法的一个趋势是为满足患者需求而寻求治愈疗法;另一趋势是对慢性传染病使用长效治疗。
抗病毒药物是传染病治疗最大的细分市场,且由于创新疗法的发展,未来将会是增长最快的传染病药物市场。据弗若斯特沙利文数据,预计中国的HBV和HIV药物市场将从2019年占总体市场的50.7%增长至2034年的78.0%。
中国对传染病药物尤其是抗病毒药物需求巨大,但目前只有很少供应。为满足巨大的治疗需求、缓解公共卫生负担,中国政府已经出台了有利的监管政策与其他措施,例如将相关疾病治疗纳入了国家医保目录,增加重大传染病(如HBV及HIV感染)的治疗可及性。另外在《健康中国2030规划》旨在加强重大传染病的防控提高国人的整体健康水平。
2019年,CNS市场为全球第四大药物市场,目前CNS药物为美国所主导。中国CNS药物还处于市场开发中,未来将保持高速增长,弗若斯特沙利文预计市场规模从2019年的296亿美元增至2034年的571亿美元。抑郁症是CNS疾病的主要类型之一。
公共卫生重大治疗领域诞生全球制药巨头
对照全球情况,已有多家国际药企的多款创新疗法产品在传染病治疗领域做出了很大贡献,企业业绩也因此受益。
首先是吉利德,先后上市了丙肝(HCV)特效药Sovaldi、Epclusa、Harvoni及Vosevi,使丙肝的治愈率大幅提升,其中Epclusa可用于全部6种基因型丙肝患者。Sovaldi和Epclusa上市后一两年内就达到了全球百亿美元销售额,Epclusa畅销后吉利德市值也较Sovaldi获批上市前市值翻了五倍。这四代产品也均在中国陆续获批。
作为抗病毒巨头之一,吉列德在乙肝、HIV治疗方面也都持续有重磅产品获批,如新型NRTI药物Viread(TDF)被广泛用于HIV和HBV的治疗;Viread的升级版产品Vemlidy(TAF)为乙肝患者提供了一种安全性大幅改善的治疗方案。吉利德的抗HIV药物Biktarvy为2020年销售额位列全球第9,当年销售额72.6亿美元,而Biktarvy是全球最小的艾滋病三联复方单片制剂,病毒抑制率达99%。吉利德市值为864亿美元。

2020年全球畅销前20药物(来源:Fiercepharma)
葛兰素史克在攻克重大传染疾病历程上也功不可没,公司在HIV和肝炎治疗市场都有成熟管线,近年在抗HIV领域有Triumeq、Tivicay等几款核心畅销产品,实现组方成分越来越小、剂量越来越小、副作用越来越低的升级。2020年,Triumeq、Tivicay的全球销售额分别为 29.8亿美元、19.73亿美元。
2021年1月,葛兰素史克又一款艾滋病新药Cabenuva在FDA获批,是首个用于成人HIV感染患者的完整长效方案,只需每月给药1次。公司市值为1018亿美元。
BRII-179、BRII-835对标国际创新疗法,公司主导中国临床试验
腾盛博药目前有13条在研管线,包括自研和合作引进的针对传染病和CNS两大类候选产品。其中,针对HBV的BRII-179为核心产品,管线进展至临床2期。
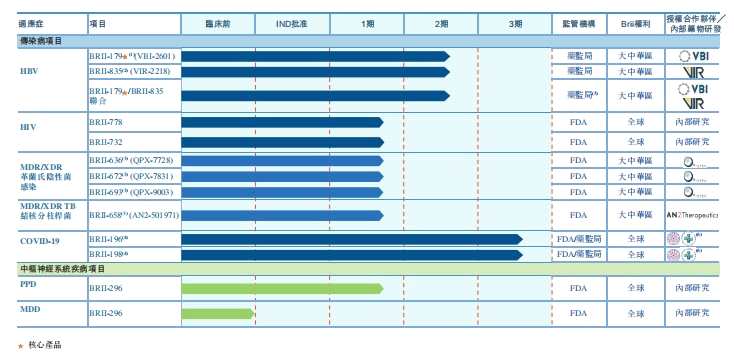
来源:招股书
BRII-179 (VBI-2601)是一种新型的基于蛋白质的重组HBV免疫治疗候选疫苗,主要针对慢性乙型肝炎病毒感染患者,它基于VBI预防性3抗原HBV疫苗候选药物的3抗原构象建立,旨在靶向增强的B细胞和T细胞免疫。
BRII-179是由腾盛博药于2018年12月从创新疫苗公司VBI Vaccines(VBIV.US)引进,腾盛博药获得了其在中国市场的商业化权益。VBI此前分别于2020年11月和2021年4月公布了1b/2a期的积极临床中期研究数据。而公司主导了BRII-179在亚洲的临床试验。
腾盛博药另一条乙肝管线BRII-835是一种针对HBV的小干扰核糖核酸(siRNA),可抑制所有乙肝病毒蛋白质的产生,尤其是乙肝病毒的表面抗原,以消除人体免疫系统针对乙肝病毒的抑制作用,也是一种高度创新的疗法。同样,BRII-835由腾盛博药获传染病创新疗法公司VirBiotechnology(VIR.US)授权联合开发,BRII-835的临床前开发及1/2期临床试验由Vir开展,腾盛博药正在中国开展BRII-835的临床2期试验。
全球来看,这种通过RNA干扰(RNAi)机制治疗乙肝的大部分管线处于临床前研究或临床早期,但也不乏先行者,如美国Arrowhead Pharmaceuticals(ARWR.US),市值88.43亿美元。Arrowhead与杨森公司联合开发了RNAi疗法JNJ-3989已经取得了一些成果,2020年8月的欧洲肝脏研究协会(EASL)肝脏大会上,研究人员宣布JNJ-3989与一种核苷(酸)类似物(NA)抗病毒疗法联用,在治疗慢性乙肝患者的2期临床试验中获得了积极结果。
与Arrowhead给药方式一样,VirBiotechnology和RNAi新药开发明星公司AlnylamPharmaceuticals(ALNY.US)合作开发的VIR-2218是另一款皮下注射,靶向肝脏递送的RNAi药物。在去年EASL肝脏大会上,据所公布的试验数据,VIR-2218在2期临床试验结果显示它可显着降低患者乙肝表面抗原水平。
HBV项目有望成为功能性治愈乙肝首创产品
我国乙肝患者数量大,乙肝恶化后有严重健康问题。与HBV相关的不公正待遇影响患者生活、经济水平。但目前干扰素几乎成为乙肝患者的唯一选择,中国的HBV治疗远未被开发。虽然乙肝目前无治愈方法,但可以实现功能性治愈,且患者自费功能性治愈的意愿较高。并且在2019年,《慢性乙型肝炎防治指南》增加了合格接受抗病毒治疗的患者群,医保已纳入HBV的创新疗法。
有别于其他仅抑制HBV复制的抗病毒疗法,腾盛博药的HBV项目有策略地专注于旨在恢复患者对HBV感染的免疫控制并实现持续病毒缓解或功能治愈而无需持续进行HBV疗法的治愈性疗法。
2021年4月,公司宣布其与Vir Biotechnology、VBI Vaccines联合开发的治疗乙肝的BRII-179(VBI-2601)与BRII-835(VIR-2218)联合疗法2期临床试验完成第一位患者给药。
腾盛博药通过结合siRNA治疗及免疫刺激性治疗疫苗的科学差异化联合疗法针对慢性HBV感染进行功能性治愈,而BRII-179与BRII-835联合疗法候选产品是首个将两种具有不同作用机制的抗乙肝药物联用的治疗方案。腾盛博药已向中国香港、新西兰、澳大利亚、台湾、新加坡、泰国及韩国相关监管机构递交BRII-179/BRII-835的2期MRCT联合研究。2021年2月,公司已向中国CDE递交BRII-179/BRII-835的2期MRCT联合研究的IND申请,预计于2021年第三季度获得批准。预计联合疗法最早2024向NMPA提交NDA。
与众多生物制药公司一样,腾盛博药目前未产生销售收入,主要支出为研发费用。2019和2020年,研发费用分别为8378.5万元和8.76亿元。(后台回复“腾盛博药”获取该公司最新招股书)
本文首发于微信公众号:IPO早知道。文章内容属作者个人观点,不代表和讯网立场。投资者据此操作,风险请自担。
盛博,药物,HBV